這篇文檔主要講了中國創新藥“出海”過程中,從研發到上市各個階段在工藝開發與生產(CMC)方面的要點和策略。具體內容如下:
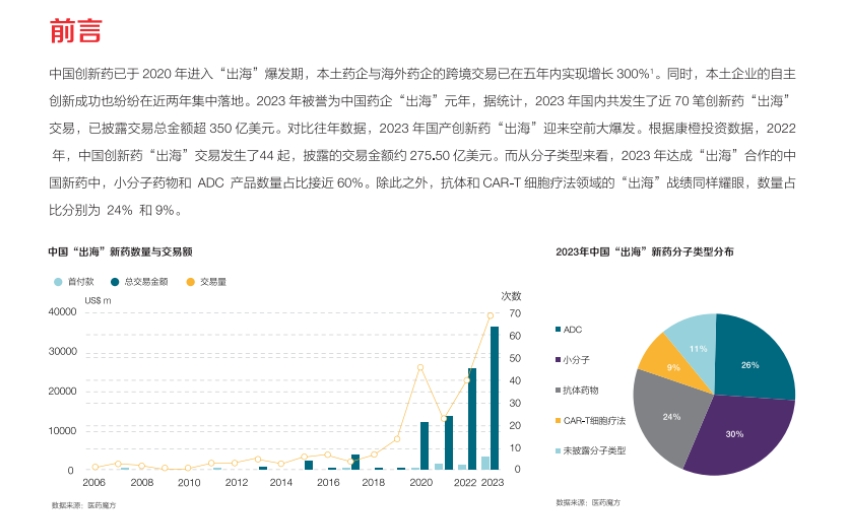
1. 中國創新藥“出海”現狀:2020年起中國創新藥進入“出海”爆發期,2023年尤為突出,交易數量和金額大幅增長,小分子藥物、ADC產品、抗體和CAR - T細胞療法等是主要“出海”的分子類型。中國藥企選擇“出海”,是因為國內市場規模有限,“出海”能接觸更多患者、多樣化監管框架、人才技術資源,還能多元化收入、降低市場風險。
2. 新藥開發到上市各階段的CMC策略
- 臨床前研究階段:要確定CMC策略、藥代動力學等,其中細胞株開發和制劑開發很關鍵。細胞株開發可采用靶向整合技術、高通量系統;制劑開發要基于平臺工藝經驗,確定最優pH等,借助創新分析方法。
- IND申報階段:提交新藥臨床研究申請時,要樹立全球觀念,編寫中立的CMC申報資料,全面評估不同管轄區要求的差距。還要建立完善的首次人體試驗(FIH)資料,加速早期制劑選擇,比如優先考慮西林瓶、凍干制劑等。
- 臨床研究階段:臨床研究階段的CMC研發周期長且不確定,需要提前規劃。臨床I - II期要合理評估生產需求,前瞻性思考生產能力,明確制劑選擇和劑量,采用靈活生產方式;臨床III期則要提前制定工藝放大計劃和技術轉移策略。
- 商業化規模生產階段:商業化生產階段,分析方法驗證、工藝表征與工藝驗證很重要。分析方法驗證前要評估穩健性,工藝表征要借助縮小模型、實驗設計等方法,工藝驗證需確定批次數量,最終提交法規監管審批。
3. 特定市場的新藥上市考量:不同國家和地區對藥品上市有特殊要求,如歐盟要明確質量授權人職責;美國要注意356h申請表、企業注冊列名;英國脫歐后需單獨申請上市許可、進行批檢驗;中國有關聯審評,對原液、輔料、驗證批次等有具體要求。
4. 總結與建議:創新藥出海企業在立項階段要有全球視野,建立全球人才體系和研發、生產及營銷體系。初創企業可借助專業第三方機構。賽默飛Patheon?能為客戶提供制藥服務解決方案。